REPORT
L’unguento KX2-391 1%, nuovo duplice inibitore del sarcoma/tubulina, è efficace e sicuro per il trattamento delle cheratosi attiniche dell’adulto secondo gli studi di fase 3
Presentato da: Edward Lain, MD, FAADAustin Institute for Clinical Research Inc., Pflugerville, TX, USA
- L’unguento KX2-391 1% è sicuro ed efficace nel trattamento delle cheratosi attiniche (AK) dell’adulto.
- L’unguento KX2-391 1% ha dimostrato l’eliminazione del 100% delle AK in almeno il 44% dei pazienti studiati.
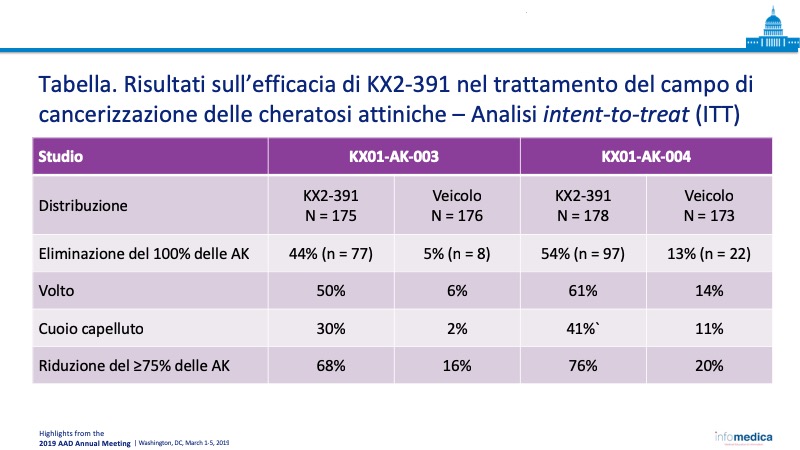
L’unguento KX2-391 1%, nuovo duplice inibitore del sarcoma (Src)/tubulina, si è dimostrato efficace nel trattamento delle AK dell’adulto in due studi di fase 3 (KX01-AK-003 e KX01-AK-004). Il risultato principale valutato nello studio è stata l’eliminazione del 100% delle AK, o la loro riduzione parziale, a livello del volto e del cuoio capelluto. L’unguento KX2-391 1% ha dimostrato un beneficio clinico statisticamente significativo rispetto al placebo, in particolare registrando l’eliminazione del 100% delle AK nel 44% dei pazienti dello studio KX01-AK-003 e nel 54% dei casi dello studio KX01-AK-004. La valutazione riguardante il profilo di sicurezza ha evidenziato che gli eventi avversi legati al trattamento (TEAE, treatment-related emergent adverse events) sono stati di entità lieve-moderata.
Obiettivo primario è stato la valutazione dell’efficacia riguardante l’eliminazione del 100% delle AK al giorno 57 e la valutazione della sicurezza, delle reazioni cutanee locali (LSR, local skin reactions) e degli eventi avversi dell’unguento KX2-391 1% in confronto al solo veicolo nei pazienti adulti con AK.
Tipo di studio
- Doppio cieco.
- Controllo con il veicolo.
- Randomizzato.
- Gruppo parallelo.
- Multicentrico.
- Fase 3.
Obiettivo primario
- Valutazione dell’efficacia nell’eliminazione del 100% delle AK al giorno 57 dell’unguento KX2-391 1% in confronto al solo veicolo nei pazienti adulti con AK.
- Valutazione della sicurezza, delle reazioni cutanee locali e degli eventi avversi dell’unguento KX2-391 1% in confronto al solo veicolo nei pazienti adulti con AK.
Popolazione dello studio
- Numero totale di pazienti arruolati: 702 soggetti in due studi identici comprendenti ciascuno 351 pazienti provenienti da 31 centri per ciascuno studio.
- Popolazione intent-to-treat.
- Età mediana: 69,75 anni.
- Sesso: rapporto maschi/femmine 6,7/1.
- 99,5% dei pazienti bianchi.
- 72,75% fototipo I/II secondo Fitzpatrick.
- Numero mediano di AK a inizio trattamento: 6.
- Area trattata: volto/cuoio capelluto 2:1.
Valutazione dell’obiettivo primario
- Valutazione dell’efficacia riguardante l’eliminazione del 100% delle AK è stata valutata al giorno 57 in un’area cutanea di 25 cm2 nei pazienti adulti con AK trattati con l’unguento KX2-391 1% in confronto al solo veicolo.
Valutazione dell’obiettivo secondario
- Valutazione della sicurezza, delle reazioni cutanee locali e degli eventi avversi dell’unguento KX2-391 1% in confronto al solo veicolo nei pazienti adulti con AK.
Farmaco/procedure utilizzate
- KX2-391 è una piccola molecola con multipli meccanismi d’azione, inclusa l’inibizione della chinasi Src e l’inibizione della polimerizzazione della tubulina che determina un incremento dell’apoptosi delle cellule in proliferazione.
- L’area trattata è stata di 25 cm2 con un numero variabile da 4 a 8 AK sul volto o sul cuoio capelluto.
- Rapporto unguento KX2-391 1% versus veicolo 1:1.
- Il trattamento è stato applicato una volta die per 5 giorni consecutivi dai partecipanti stessi e lasciato in sede per circa 12 ore.
- L’aderenza al trattamento è stata maggiore del 99%.
- I risultati hanno dimostrato un’efficacia statisticamente significativa di KX2-391 rispetto al solo veicolo (Tabella).
- I risultati relativi alla sicurezza hanno dimostrato che KX2-391 è stato ben tollerato.
- L’esposizione oculare non ha determinato la comparsa di eventi avversi (EA) a livello oculare.
- Non sono stati rilevati cambiamenti clinicamente significativi all’ECG o variazione all’esame obiettivo fisico o dei parametri vitali e di laboratorio correlati alla terapia.
- Tutti gli EA gravi occorsi durante lo studio non stati considerati correlati al trattamento.
- Le percentuali di aventi avversi legati al trattamento emerse durante il trattamento sono state dell’11-20% nel gruppo trattato con il farmaco contro il 9-11% nel gruppo che ha utilizzato il solo veicolo.
- I principali EA locali (mean composite LSR score 4) sono emersi al giorno 8 e si sono risolti in media entro il giorno 29.
- I più comuni EA locali sono stati eritema, esfoliazione e desquamazione.
- L’unguento KX2-391 1% si è dimostrato sicuro ed efficace in due identici trial clinici di fase 3, dimostrando più alti tassi globali di riduzione completa delle AK al giorno 57, con il 44% e il 54% di pazienti che hanno raggiunto l’eliminazione del 100% delle lesioni.
- Le differenze cliniche sono risultate statisticamente significative per tutti i sottogruppi analizzati, incluso il cuoio capelluto e il volto.
- La maggior parte dei TEAE hanno incluso reazioni locali quali prurito e dolore, di grado lieve-moderato che non hanno richiesto alcun trattamento.
- L’aderenza al trattamento dei partecipanti è stata eccellente e più del 99% dei pazienti ha completato il trattamento di 5 giorni.
Messaggi chiave/prospettive cliniche
- L’unguento KX2-391 1% si è dimostrato sicuro ed efficace per il trattamento delle cheratosi attiniche dell’adulto.
- Circa la metà (rispettivamente il 44 e il 54%) dei pazienti ha ottenuto un’eliminazione completa del 100% delle lesioni con un miglioramento maggiore nel volto.
- I risultati sulla sicurezza hanno dimostrato che la maggior parte TEAE sono stati lievi-moderati e non hanno richiesto alcun trattamento.
Presenter disclosure(s): The presenter has reported that he is an investigator for this clinical trial, and that the study is sponsored by Athenex, Inc. The content of the presentation had not been publicly disclosed as of the AAD 2019 presentation, and was provided for research purposes only. Almirall and Athenex are partners in the development program of KX2-391 ointment 1% for actinic keratosis.
Written by: Daniel Bennett, MPH
Reviewed by: Martina Lambertini, MD
TUTTI I REPORT

Benvenuti agli Highlights di AAD 2019
Prof. Nellie Konnikov, MD, FAADSiamo lieti di presentare gli Highlights dell’Annual Meeting 2019 dell’American Academy of Dermatology (AAD). Il meeting si è tenuto quest’anno dal 1 al 5 marzo a Washington, DC, e ha messo in luce … [ Leggi tutto ]

 amèrica latina
amèrica latina Canada EN
Canada EN Canada FR
Canada FR Deutschland
Deutschland English
English português
português Taiwan
Taiwan