ZUSAMMENFASSUNGEN
ALOPECIA AREATA
Die oralen Januskinase-Inhibitoren PF-06700841 und PF-06651600 bieten eine klinisch nachweisbare therapeutische Wirksamkeit nach 4 und 6 Wochen bei Patienten mit Alopecia areata und eine noch stärkere Wirksamkeit nach 24 Wochen bei Patienten mit kürzerer Dauer des aktuellen Alopezie-Schubs: Ergebnisse einer randomisierten Phase-IIa-Studie
Vorgetragen von: Elena Peeva, MD, MSc, FACRCambridge, MA, USA
- Die oralen Januskinase-(JAK)-Inhibitoren PF-06700841 und PF-06651600 zeigen bei Patienten mit Alopecia areata (AA) einen Wirkungseintritt nach 6 Wochen.
- Aus den Subgruppenanalysen geht hervor, dass für die Dauer des AA-Schubs spezifische klinische Baseline-Merkmale den Therapieerfolg beeinflussen.
In dieser klinischen Phase-IIa-Studie wurden der orale Tyrosinkinase-2-(TYK2)-/JAK1-Inhibitor PF-06700841 und der orale JAK3-Inhibitor PF-06651600 bei mittelschwerer bis schwerer AA untersucht. Bei den beiden Therapien und bei Placebo wurden die für den Zeitpunkt des Wirkungseintritts spezifischen Ergebnismessgrößen verglichen. Außerdem wurden Subgruppenanalysen zu klinischen Merkmalen, die spezifisch für den AA-Typ sind, sowie zur Dauer durchgeführt.
- Die Beurteilung des Wirkungseintritts des oralen TYK2-/JAK1-Inhibitors PF-06700841 und des oralen JAK3-Inhibitors PF-06651600 bei mittelschwerer bis schwerer AA.
- Die Beurteilung der Dauer des AA-Schubs und des Zusammenhangs mit der Wirksamkeit von PF-06700841 und PF-06651600 über einen Zeitraum von 24 Wochen.
Art der Studie
- Doppelblind.
- Randomisiert.
- Multizentrisch.
- Phase IIa.
- Zwei noch nicht abgeschlossene Verlängerungsstudien.
Hauptziel
- Hauptziel der Studie war die Beurteilung des oralen TYK2-/JAK1-Inhibitors PF-06700841 und des oralen JAK3-Inhibitors PF-06651600 bei mittelschwerer bis schwerer AA.
- Untersucht wurden der Wirkungseintritt und die Dauer des AA-Schubs.
Patientenpopulationen
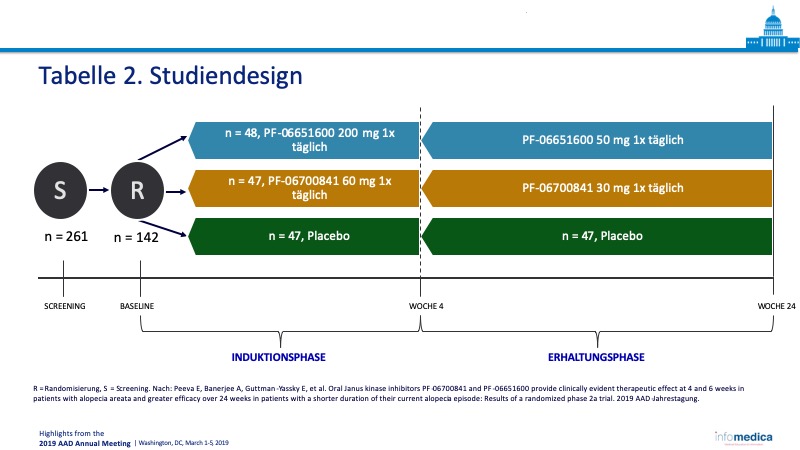
- Anzahl der Teilnehmer insgesamt: 142 Patienten in drei Kohorten, PF-06700841 (n = 47), PF-06651600 (n = 48) und Placebo (n = 47).
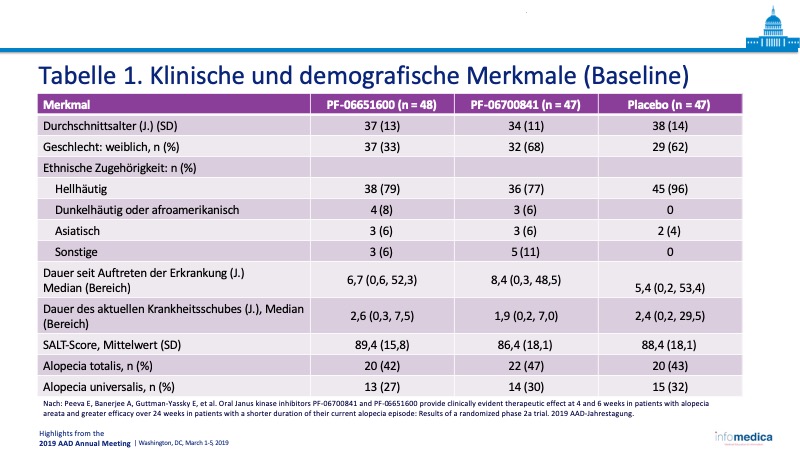
- Alter: Patienten im Alter von 18–75 Jahren in drei Kohorten, mit einem durchschnittlichen Alter von jeweils 37 Jahren, 34 Jahren und 38 Jahren.
- Intent-to-Treat-Population.
- Mittelschwere bis schwere AA (> 50 % Haarausfall an der Kopfhaut).
- Einschließlich Patienten mit Alopecia totalis und Alopecia universalis.
- Tabelle 1: klinische und demografische Merkmale der Patienten.
Primäre Ergebnismessgrößen
- Die primäre Ergebnismessgröße war der Score im Severity of Alopecia Tool (SALT) zur Messung des Schweregrads der Alopezie, mit einer Längsschnittanalyse der Veränderung gegenüber Baseline zur Ermittlung des ersten statistisch signifikanten Unterschieds, wobei PF-06700841, PF-06651600 und Placebo verglichen wurden.
Sekundäre Ergebnismessgrößen
- Die sekundäre Ergebnismessgröße war die Subgruppenanalyse des SALT-Scores hinsichtlich der langfristigen Veränderung gegenüber Baseline, wobei PF-06700841, PF-06651600 und Placebo verglichen wurden, um die Auswirkungen der Dauer des aktuellen AA-Schubs auf die Wirksamkeit zu vergleichen.
Angewendete Arzneimittel/Verfahren
- Die Patienten wurden drei Kohorten zugeordnet und über den Studienzeitraum von 24 Wochen mit PF-06700841, PF-06651600 oder Placebo behandelt (Tabelle 2).
- Die folgenden klinischen Baseline-Merkmale wurden u. a. untersucht: Dauer seit dem erstmaligem Auftreten der Erkrankung; Dauer des aktuellen Krankheitsschubs; SALT-Score und, ob der Teilnehmer an AA, Alopecia totalis oder Alopecia universalis litt.
- Der SALT-Score wurde in regelmäßigen Abständen erhoben und es wurden Zusammenhänge zwischen klinischen Merkmalen, der Dauer der Erkrankung und der untersuchten Behandlungskohorte erfasst.
- Bei der Ergebnismessgröße der Veränderung des SALT-Scores lag der mittlere Unterschied zu Placebo nach 4 Wochen bei 7,7 bei PF-06700841 und bei 2,9 bei PF-06651600.
- Der mittlere Unterschied gegenüber Placebo betrug nach 6 Wochen 19,6 bei PF-06700841 und 12,6 bei PF-06651600.
- Die Subgruppenanalyse ergab nach 24 Wochen bei einer Stratifizierung nach Schubdauer eine Veränderung des SALT-Scores gegenüber Baseline im Vergleich zu Placebo von 53,4 bei PF-06700841 und von 42,1 bei PF-06651600 bei Teilnehmern mit einem aktuellen AA-Schub von < 3,5 Jahren.
- Bei Patienten mit einem aktuellen AA-Schub von ≥ 3,5 Jahren lag die Veränderung des SALT-Scores nach 24 Wochen gegenüber Baseline im Vergleich zu Placebo bei 39,1 bei PF-06700841 und bei 22,7 bei PF-06651600.
- Die sekundäre Ergebnismessgröße der Beurteilung des Einflusses der aktuellen Schubdauer auf die Wirksamkeit ergab somit ein stärkeres Ansprechen innerhalb von 24 Wochen bei Patienten mit kürzerer Dauer des aktuellen AA-Schubs.
- Der orale TYK2-/JAK1-Inhibitor PF-06700841 und der orale JAK3-Inhibitor PF-06651600 haben bei mittelschwerer bis schwerer Alopecia areata einen Wirkungseintritt von 4 Wochen und 6 Wochen.
- Das nach 24 Wochen gemessene Ansprechen kann bei Teilnehmern größer sein, die bei Baseline eine kürzere Dauer des aktuellen Schubs der Alopecia areata aufweisen.
Kernaussagen/klinische Perspektiven
- Die Daten der Phase-II-Studie zum oralen TYK2-/JAK1-Inhibitor PF-06700841 und zum oralen JAK3-Inhibitor PF-06651600 deuten darauf hin, dass diese mit einem Wirkungseintritt nach jeweils 4 und 6 Wochen bei mittelschwerer bis schwerer Alopecia areata eine frühere Wirksamkeit als vorherige Therapien aufweisen.
- Die nach klinischen Merkmalen durchgeführten Subgruppenanalysen zeigen, dass das Ansprechen bei Patienten mit kürzerer Krankheitsdauer stärker sein kann.
Presenter disclosure(s): The presenter has reported the following disclosure: Pfizer Inc.
Written by: Daniel Bennett, MPH
Reviewed by: Martina Lambertini, MD
CONFERENCE SUMMARIES

WILLKOMMEN ZU DEN AAD HIGHLIGHTS
Prof. Nellie Konnikov, MD, FAADWir freuen uns, Ihnen die Highlights der Jahrestagung 2019 der American Academy of Dermatology (AAD) vorzustellen. Die Tagung fand vom 1. bis 5. März 2019 in Washington (DC) statt. Zu den Höhepunkten der AAD-Konferenz zählten u. a. … [ MEHR LESEN ]

 amèrica latina
amèrica latina Canada EN
Canada EN Canada FR
Canada FR English
English italiano
italiano português
português Taiwan
Taiwan