REPORT
Clascoterone topico in crema 1%: un nuovo antiandrogeno topico, locale e selettivo: risultati di due studi di fase 3 per il trattamento dell’acne del volto in bambini e adulti
Presentato da: Adelaide A. Hebert, MD, FAADProfessor, Department of Dermatology
UTHealth McGovern Medical School, Houston, TX, USA
- Il clascoterone è il primo inibitore del recettore degli androgeni topico ed è disponibile in due formulazioni. Sono in corso di sperimentazione una crema all’1% per l’acne e una soluzione al 7.5% per l’alopecia androgenetica.
- Ci sono stati risultati positivi di fase 3 per l’acne e risultati positivi di fase 2 per l’alopecia androgenetica.
- È stato dimostrato un buon profilo di sicurezza su più di 1700 pazienti.
Il clascoterone è un inibitore del recettore degli androgeni topico in corso di sperimentazione per il trattamento dell’acne. Il clascoterone viene idrolizzato dalla pelle e metabolizzato in cortexolone-21-propionato e cortexolone. Entrambi i metaboliti mostrano minima attività antiandrogenica e deboli proprietà glucocorticoidi [1,2]. Il cortexolone è il composto finale che ha un profilo stabilito di sicurezza [1,2]. Tale agente è diretto contro i recettori degli androgeni nei sebociti e nelle cellule della papilla del follicolo all’interno dell’unità pilosebacea, interviene in molteplici punti differenti della patogenesi dell’acne ed inibisce la via di segnalazione dei recettori degli androgeni stimolata dal diidrotestosterone.
- L’obiettivo primario dello studio è stata la valutazione dell’efficacia del clascoterone topico 1% crema per il trattamento dell’acne del volto nei bambini e negli adulti.
- Lo studio ha determinato la riduzione percentuale delle lesioni infiammatorie e non infiammatorie del volto in 12 settimane.
Tipo di studio
- Fase 3.
- Randomizzato.
- Doppio cieco.
- Confronto con il veicolo.
- Multicentrico.
- Due studi identici (25 e 26) in 112 centri.
Obiettivo primario
- L’obiettivo primario dello studio è stata la valutazione dell’efficacia del clascoterone topico 1% crema per il trattamento dell’acne del volto nei bambini e negli adulti.
- Lo studio ha determinato la riduzione percentuale delle lesioni infiammatorie e non infiammatorie del volto in 12 settimane.
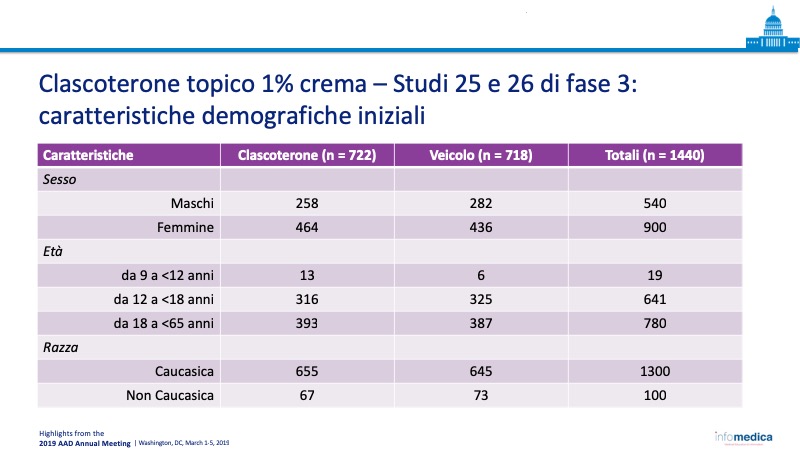
Popolazioni dei pazienti
- Numero totale di soggetti arruolati: 1440 pazienti.
- Età: ≥9 anni.
- Popolazione: intent-to-treat.
- Criteri di inclusione:
- 30-75 lesioni infiammatorie e 30-100 lesioni non infiammatorie.
- Scala IGA a 5 punti – moderata o severa (gradi 3 o 4).
- Criteri di esclusione:
- Pazienti in gravidanza, allattamento o con l’intenzione di pianificare una gravidanza durante lo studio.
- Pazienti con patologie cutanee che potrebbero interferire con la valutazione dei prodotti testati o che necessitano di trattamenti topici o sistemici che danno interferenza.
- Soggetti con più di 2 noduli.
- Soggetti con acne nodulocistica.
- Soggetti con condizioni che lo sperimentatore reputa potrebbero non essere sicure per il paziente che partecipa allo studio.
- Soggetti al momento arruolati in studi su farmaci o dispositivi.
- Soggetti che hanno assunto un farmaco sperimentale o che hanno partecipato a sperimentazioni di dispositivi nei 30 giorni precedenti l’inizio del trattamento.
- Nella Tabella sono riportate le caratteristiche cliniche e demografiche dei pazienti.
Valutazione dell’obiettivo primario
- Cambiamento nell’acne del volto, evidenziato dalla modificazione percentuale delle lesioni infiammatorie a 12 settimane, al fine di valutare una variazione statisticamente significativa dall’inizio del trattamento tra il clascoterone topico 1% in crema ed il veicolo.
Valutazione dell’obiettivo secondario
- Cambiamento nell’acne del volto, evidenziato dalla modificazione percentuale delle lesioni non infiammatorie a 12 settimane, al fine di valutare una variazione statisticamente significativa dall’inizio del trattamento tra il clascoterone topico 1% in crema e il veicolo.
Farmaci/procedure utilizzati
- È stato condotto uno studio di fase 3 di 12 settimane in soggetti di età ≥9 anni con acne moderata-severa, seguito da un’estensione aperta di 9 mesi sulla sicurezza.
- I pazienti sono stati assegnati in maniera casuale al clascoterone topico 1% in crema o al veicolo (1:1) per un trattamento di 12 settimane, durante il quale il paziente doveva applicare il trattamento 2 volte die, mattino e sera.
- Gli obiettivi primari valutati sono stati la proporzione di pazienti in ciascun gruppo con riduzione di almeno due punti della IGA rispetto all’inizio del trattamento e uno score IGA di 0 (completo) oppure 1 (quasi completo) a 12 settimane.
- Nel paziente è stato valutato un cambiamento assoluto dall’inizio del trattamento a 12 settimane delle lesioni sia infiammatorie sia non infiammatorie.
- Relativamente all’obiettivo delle lesioni non infiammatorie a 12 settimane, la coorte trattata con clascoterone topico 1% crema ha mostrato una riduzione del 28,9% rispetto alla riduzione del 18,9% del veicolo, evidenziando un miglioramento statisticamente significativo.
- Relativamente all’obiettivo delle lesioni infiammatorie a 12 settimane, la coorte trattata con clascoterone topico 1% crema ha mostrato una riduzione del 46,2% rispetto alla riduzione del 32,7% del veicolo, evidenziando un miglioramento statisticamente significativo.
- Gli effetti collaterali legati al trattamento (TEAE, treatment-emergent adverse events) sono stati dell’11,1% per la coorte del clascoterone (2,6% moderati, nessuno severo) rispetto al 12,7% della coorte del veicolo (4,3% moderati, <1% severi). Le reazioni cutanee locali sono state caratterizzate da lieve eritema.
- Il trattamento con clascoterone topico 1% crema ha mostrato una riduzione clinicamente significativa sia delle lesioni infiammatorie sia non infiammatorie a 12 settimane sia nei bambini sia negli adulti, dimostrandosi pertanto efficace.
- Il trattamento con clascoterone topico 1% crema ha determinato un basso tasso di TEAE, generalmente non severi, dimostrandosi pertanto sicuro.
Messaggi chiave/prospettive cliniche
- I dati di fase 3 sul clascoterone topico 1% crema hanno dimostrato l’efficacia nel trattamento dell’acne del volto nei pazienti adulti e nei bambini di età ≥9 anni.
- I dati di fase 3 sul clascoterone topico 1% crema hanno dimostrato un profilo di sicurezza tollerabile nel trattamento dell’acne del volto nei pazienti adulti e nei bambini di età ≥9 anni.
REFERENZE
Presenter disclosure(s): The presenter has reported the following disclosures: Allergan, Inc.; Amgen; Anacor Pharmaceuticals, Inc.; Astellas Pharma US, Inc.; Bickel Biotechnology; Cassiopia; Celgene Corporation; Chugai Pharma; Cutanea Life Sciences; US, Department of Defense; Dermavant Sciences; Dermira; Encore Dermatology, Inc.; Galderma Laboratories, L.P.; GlaxoSmithKline; Intendis, Inc.; La Roche-Posay Laboratoire Pharmaceutique; Mayne Pharma Group; Medimetriks Pharmaceuticals, Inc.; Menarini Group; Menlo Therapeutics; Merz Pharmaceuticals, LLC; NIH; Novan; Novartis Pharmaceuticals Corp.; Onset Therapeutics Ortho Dermatologics; Pfizer Inc.; Pharmaderm; PPD Inc.; Prim-Med; Promius Pharma, LLC; Promius Pharmaceuticals; Regeneron; Roivant Sciences; Shionogi USA; Sienna Biopharmaceuticals; Sinclair Pharma; Stiefel, a GSK company; TopMD; Valeant Pharmaceuticals International; Vanda Pharmaceuticals Inc.
Written by: Daniel Bennett, MPH
Reviewed by: Martina Lambertini, MD
TUTTI I REPORT

Benvenuti agli Highlights di AAD 2019
Prof. Nellie Konnikov, MD, FAADSiamo lieti di presentare gli Highlights dell’Annual Meeting 2019 dell’American Academy of Dermatology (AAD). Il meeting si è tenuto quest’anno dal 1 al 5 marzo a Washington, DC, e ha messo in luce … [ Leggi tutto ]

 amèrica latina
amèrica latina Canada EN
Canada EN Canada FR
Canada FR Deutschland
Deutschland English
English português
português Taiwan
Taiwan