RÉSUMÉS
Crème topique de clascotérone à 1 %, un nouvel anti-androgénique sélectif topique : Résultats de deux études de phase 3 sur le traitement de l’acné vulgaire au visage chez des patients pédiatriques et adultes
Présenté par: Adelaide A. Hebert, MD, FAADProfessor, Department of Dermatology
UTHealth McGovern Medical School, Houston, TX, USA
- La clascotérone est le premier inhibiteur topique des récepteurs des androgènes et existe sous deux formes : une crème à 1 % est à l’étude pour l’acné et une solution à 7,5 % est à l’étude pour l’alopécie androgénique.
- On a obtenu des résultats favorables de phase 3 pour l’acné, et des résultats favorables de phase 2 pour l’alopécie androgénique.
- Un profil d’innocuité net a été démontré chez plus de 1 700 patients.
La clascotérone est un inhibiteur topique des récepteurs des androgènes à l’étude pour le traitement de l’acné. La clascotérone est hydrolysée par la peau et métabolisée en 21-propionate de cortexolone et en cortexolone. Les deux métabolites manifestent une activité anti-androgénique minimale et ont de faibles propriétés glucocorticoïdes [1,2]. La cortexolone est la molécule finale qui a un profil d’innocuité établi [1,2]. Cet agent cible les récepteurs des androgènes dans les sébocytes et les cellules du derme papillaire dans l’unité pilosébacée; il intervient en différents points de la pathogenèse de l’acné et inhibe la transmission des signaux des récepteurs des androgènes modulée en aval par la dihydrotestostérone.
- L’objectif principal de l’étude était d’évaluer l’efficacité de la crème topique de clascotérone à 1 % pour le traitement de l’acné vulgaire au visage chez des populations adultes et pédiatriques.
- L’étude a évalué la réduction en pourcentage des lésions inflammatoires et non inflammatoires au visage sur une période de 12 semaines.
Type d’étude
- Phase 3.
- Randomisée.
- À double insu.
- Avec témoins sous excipient.
- Multicentrique.
- Deux études identiques (25 et 26) dans 112 sites.
But principal
- Le but principal de l’étude était d’évaluer l’efficacité de la crème topique de clascotérone à 1 % pour le traitement de l’acné vulgaire au visage chez des populations adultes et pédiatriques.
- L’étude a évalué la réduction en pourcentage des lésions inflammatoires et non inflammatoires au visage sur une période de 12 semaines.
Populations de patients
- Nombre total de patients recrutés : 1 440 patients.
- Âge: ≥ 9 ans.
- Population en intention de traiter.
- Critères d’inclusion:
- 30-75 lésions inflammatoires et 30-100 lésions non inflammatoires.
- Échelle en 5 points d’évaluation globale par l’investigateur (IGA) - modérée ou grave (grade 3 ou 4).
- Critères d’exclusion:
- Femme enceinte, qui allaite ou planifie une grossesse pendant la période de l’étude.
- Patient ayant une maladie dermatologique susceptible d’interférer avec l’évaluation des produits testés ou nécessitant le recours à un traitement topique ou systémique intercurrent.
- Patient ayant plus de 2 nodules au visage.
- Patient souffrant d’acné nodulokystique.
- Patient ayant une maladie qui, de l’avis de l’investigateur, compromettrait sa sécurité s’il participait à l’étude.
- Patient actuellement inscrit à une étude sur un médicament ou un dispositif expérimental.
- Patient ayant reçu un médicament expérimental ou ayant testé un dispositif expérimental dans les 30 jours précédant le début du traitement (départ).
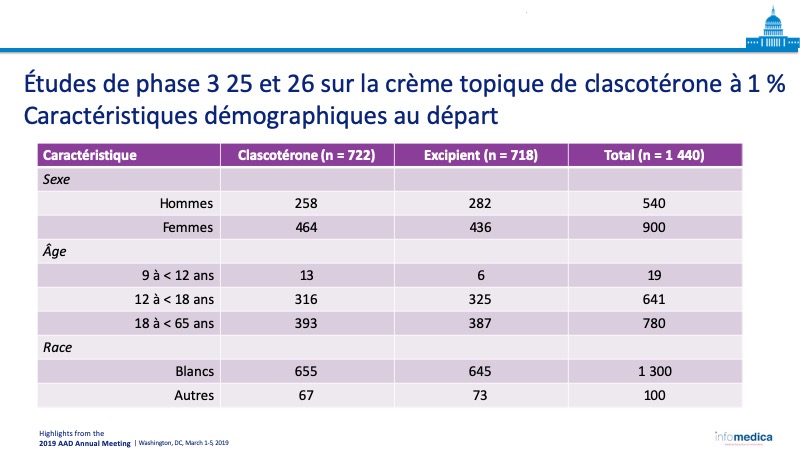
- Le tableau présente les caractéristiques cliniques et démographiques des patients.
Paramètre principal
- Le paramètre principal était l’évaluation des changements de l’acné vulgaire au visage, mesurés en pourcentage de modification des lésions inflammatoires à la semaine 12, afin de déterminer une amélioration par rapport aux valeurs de départ et le cas échéant, une différence statistiquement significative entre la crème topique de clascotérone à 1 % et l’excipient.
Paramètres secondaires
- Le paramètre secondaire était l’évaluation des changements de l’acné vulgaire au visage, mesurés en pourcentage de modification des lésions non inflammatoires à la semaine 12, afin de déterminer une amélioration par rapport aux valeurs de départ et le cas échéant, une différence statistiquement significative entre la crème topique de clascotérone à 1 % et l’excipient.
Médicaments/interventions utilisés
- Étude de 12 semaines de phase 3 menée auprès de sujets de ≥ 9 ans atteints d’acné de modérée à grave, suivie d’un volet d’évaluation de l’innocuité à étiquetage en clair d’une durée de neuf mois.
- Les patients ont été assignés aléatoirement à la crème topique de clascotérone à 1 % ou à l’excipient en crème (1:1) pour un traitement de 12 semaines durant lequel ils devaient appliquer eux-mêmes la crème deux fois par jour, matin et soir.
- Les coparamètres principaux d’efficacité évalués étaient la proportion de sujets de chaque groupe ayant obtenu une réduction d’au moins deux points à l’échelle d’évaluation globale par l’investigateur (IGA) par rapport aux valeurs de départ et un score IGA de 0 (élimination des lésions) ou 1 (quasi-élimination des lésions) à la semaine 12.
- Les participants ont été évalués au plan du changement absolu des lésions non inflammatoires et inflammatoires vs départ à la semaine 12.
- Pour le paramètre des lésions non inflammatoires à la semaine 12, la cohorte traitée au moyen de la crème topique de clascotérone à 1 % a obtenu une réduction de 29,8 %, contre 18,9 % pour le groupe soumis à l’excipient, soit une amélioration statistiquement significative.
- Pour le paramètre des lésions inflammatoires à la semaine 12, la cohorte traitée au moyen de la crème topique de clascotérone à 1 % a obtenu une réduction de 46,2 %, contre 32,7 % pour le groupe soumis à l’excipient, soit une amélioration statistiquement significative.
- Les effets indésirables liés au traitement (EILT) se sont manifestés chez 11,1 % des sujets sous clascotérone (2,6 % modérés, aucun grave), contre 12,7 % des sujets ayant reçu l’excipient (4,3 % modérés, < 1 % graves). Les réactions cutanées locales ont été des érythèmes légers.
- Le traitement au moyen de la crème topique de clascotérone à 1 % a donné lieu à une réduction cliniquement significative des lésions cutanées inflammatoires et non inflammatoires sur 12 semaines chez les enfants et les adultes, ce qui atteste de son efficacité.
- Le traitement au moyen de la crème topique de clascotérone à 1 % a donné lieu à un taux faible d’EILT qui en général ont été bénins, ce qui atteste de son innocuité.
Messages clés et perspectives cliniques
- Les données de l’étude de phase 3 sur la crème topique de clascotérone à 1 % montrent qu’elle est efficace pour le traitement de l’acné vulgaire au visage chez les populations adultes et pédiatriques à partir de l’âge de 9 ans.
- Les données de l’étude de phase 3 sur la crème topique de clascotérone à 1 % montrent qu’elle a un profil d’innocuité tolérable lorsqu’elle est utilisée pour le traitement de l’acné vulgaire au visage chez les populations adultes et pédiatriques âgées de ≥ 9 ans.
RÉFÉRENCES
Presenter disclosure(s): The presenter has reported the following disclosures: Allergan, Inc.; Amgen; Anacor Pharmaceuticals, Inc.; Astellas Pharma US, Inc.; Bickel Biotechnology; Cassiopia; Celgene Corporation; Chugai Pharma; Cutanea Life Sciences; US, Department of Defense; Dermavant Sciences; Dermira; Encore Dermatology, Inc.; Galderma Laboratories, L.P.; GlaxoSmithKline; Intendis, Inc.; La Roche-Posay Laboratoire Pharmaceutique; Mayne Pharma Group; Medimetriks Pharmaceuticals, Inc.; Menarini Group; Menlo Therapeutics; Merz Pharmaceuticals, LLC; NIH; Novan; Novartis Pharmaceuticals Corp.; Onset Therapeutics Ortho Dermatologics; Pfizer Inc.; Pharmaderm; PPD Inc.; Prim-Med; Promius Pharma, LLC; Promius Pharmaceuticals; Regeneron; Roivant Sciences; Shionogi USA; Sienna Biopharmaceuticals; Sinclair Pharma; Stiefel, a GSK company; TopMD; Valeant Pharmaceuticals International; Vanda Pharmaceuticals Inc.
Written by: Daniel Bennett, MPH
Reviewed by: Martina Lambertini, MD
SOMMAIRE

Bienvenue sur AAD 2019
Prof. Nellie Konnikov, MD, FAADNous sommes heureux de vous présenter les faits saillants du Congrès annuel 2019 de l’American Academy of Dermatology (AAD). La rencontre s’est déroulée du 1er au 5 mars 2019 à Washington, DC. Les faits saillants … [ Tout lire ]

 amèrica latina
amèrica latina Canada EN
Canada EN Deutschland
Deutschland English
English italiano
italiano português
português Taiwan
Taiwan